I. Tujuan
- Mengetahui cara pembuatan tawas
- Meminimalisir limbah alumunium foil dan kaleng
- Mengetahui tawas yang baik
Aluminium sulfat
padat dengan nama lain: alum, alum padat, aluminium alum, cake alum, atau
aluminium salt adalah produk buatan berbentuk bubuk, butiran, atau bongkahan, dengan rumus kimia Al2(SO4)3.
xH2O. Kekeruhan dalam air dapat
dihilangkan melalui penambahan sejenis bahan kimia yang disebut koagulan. Pada
umumnya bahan seperti Aluminium sulfat [Al2(SO4)3.18H2O]
atau sering disebut alum atau tawas, fero sulfat, Poly Aluminium Chlorida (PAC)
dan poli elektrolit organik dapat digunakan
sebagai koagulan. Untuk menentukan dosis yang optimal, koagulan yang sesuai dan
pH yang akan digunakan dalam proses penjernihan air, secara sederhana dapat
dilakukan dalam laboratorium dengan menggunakan tes yang sederhana (Alearts
&Santika, 1984).
Tawas kalium aluminium sulfat dihasilkan dengan
mereaksikan logam aluminium (Al) dalam larutan basa kuat (kalium hidroksida)
akan larut membentuk aluminat menurut persamaan reaksi 1)
2Al (s) + 2KOH (aq) + 2H2O(l) à 2KAlO2
(aq) + 3H2 (g) ---------- (1)
Kadang–kadang ditulis dalam bentuk ion sebagai
kompleks aluminat yang persamaan reaksinya 2)
2Al (s) + 2OH– (aq) + 6H2O (l) à 2 Al(OH)4-
(g) + 3H2 (g) ---- (2)
Larutan aluminat dinetralkan dengan asam sulfat
mula-mula terbentuk endapan berwarna putih dari aluminium hidroksida [Al(OH)3],
yang dengan penambahan asam sulfat enadapan putih semakin banyak dan jika asam
sulfat berlebihan endapan akan larut membentuk kation K+, Al3+,
dan SO42-, yang jika didiamkan akan terbentuk krital
seperti kaca dari tawas kalium aluminium sulfat atau sering disebut alum.
Secara singkat reaksi yang terjadi dapat dituliskan sebagai berikut.
2KAlO2(aq) + 2 H2O(l)+
H2SO4(aq) à K2SO4(aq) + 2Al(OH)3(s)
........... (3)
H2SO4(aq) + K2SO4
(aq) + 2 Al(OH)3 (s) à 2 KAl(SO4)2 (aq) + 6H2O
............(4)
24 H2O (l) + 2 KAl(SO4)2
à 2 KAl(SO4)2.12
H2O (s) ..................(5)
Reaksi keseluruhan
2Al(s) + 2KOH(aq) + 10H2O(l) + 4H2SO4(aq)
à 2KAl(SO4)2.12H2O(s)
+ 3H2(g). ................... (6)
Larutan di persamaan (2) dipanaskan pada suhu 60-800C
untuk menguapkan airnya dan suhu pemanasan tidak boleh lebih dari 800C
karena tawas akan larut dalam air mendidih. Pada proses penguapan selama 10
menit dan didinginkan akan terbentuk kristal dari KAl(SO4)2.12H2O.
Senyawa aluminium
khususnya senyawa sulfat banyak digunakan pada industri kertas Selain itu,
tawas digunakan sebagai koagulan dalam pengolahan air dan air buangan maupun penyamakan kulit dan bahan pewarna di industri
tekstil. Namun tawas natrium yang kita buat kali ini juga dapat digunakan
sebagai bahan pengembang roti. Selain itu tawas pun dapat digunakan untuk
mengentalkan lateks (getah karet yang cair) sehingga menjadi membeku.
Beberapa contoh tawas, cara membuat dan kegunaannya:
- Natrium aluminium sulfat dodekahidrat (tawas natrium) dengan formula NaAl(SO4)2.12H2O digunakan sebagai serbuk pengembang roti.
- Kalium aluminium sulfat dodekahidrat (tawas kalium) dengan rumus KAl(SO4)2.12H2O digunakan dalam pemurnian air, pengolahan limbah, dan bahan pemadam api. Tawas kalium dibuat dari logam aluminium dankalium hidroksida. Logam aluminium bereaksi secara cepat dengan KOH panas menghasilkan larutan garam kalium aluminat.
- Amonium aluminium sulfat dodekahidrat (tawas amonium) dengan formula NH4Al(SO4)2.12H2O digunakan sebagai acar ketimun.
- Kalium kromium (III) sulfat dodekahidrat (tawas kromium) dengan formula KCr(SO4)2.12H2O digunakan sebagai penyamak kulit dan bahan pembuatkain tahan api
- Amonium besi (III) sulfat dodekahidrat (tawas besi(II)) dengan formula NH4Fe(SO4)2.12H2O digunakan untuk mordan pada pewarnaan tekstil. Tawas ini dibuat dengan mengoksidasi ion besi (II) menjadi ion besi (III) dengan asam nitrat dalam larutan amonium sulfat.
Untuk setiap kali
pembuatan tawas, sebagian pelarut mungkin perlu dikurangi dengan cara penguapan untuk
menghasilkan larutan jenuh yang kemudian menghasilkan kristal tawas pada waktu didinginkan. Untuk
mendapatkan kristal yang berukuran besar, pendinginan larutan jenuh harus dilakukan
secara pelan-pelan.
III. Alat dan Bahan
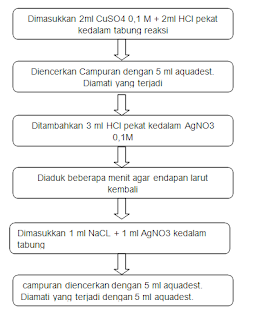
IV. Cara Kerja
III. Alat dan Bahan
Alat
- Erlenmeyer
- Gelas Ukur
- Cawan Petri
- Gelas beaker
- Corong
- Kertas saring
- Gunting
- Pipet
Bahan
- Alumunium foil
- KOH
- Accu
- Etanol
- Es batu
IV. Cara Kerja
V. Hasil Pengamatan
Berat alumunium foil : 1 gram
Berat tawas yang dihasilkan : 5 gram
Berat tawas murni yang dihasilkan: 10,4453 gram
VI. Pembahasan
Pada praktikum ini akan membahas tentang pembuatan dan pengujian tawas yang terbuat dari limbah alumunium foil dan kaleng. Tawas dapat dibuat dari logam Al yang kemudian dilarutkan kedalam KOH dan seterusnya direaksikan dengan asam sulfat yang akan menghaislkan endapan. Pada praktikum kali ini kita menggunakan Alumunium foil yang sejatinya hanya dapat sigunakan sekali saja dan setelah itu akan menjadi limbah. Dengan kata lain kita dapat memanfaatkan limbah alumunium foil menjadi tawas yang bermanfaat dan memiliki nilai jual di industri.
Proses awal pembuatan tawas adalah dengan memotong kecil kecil alumunium foil yang hendak dipakai, dengan tujuan agar reaksi yang terjadi antara alumunium foil dan KOH berlangsung lebih cepat karena salah satu faktor yang dapat memepengaruhi laju reaksi adalah luas permukaan. Semakin besar luas permuaan maka semakin cepat pula reaksi itu berlangsung. Reaksi alumunium dengan KOH bersifat eksoterm karena menghasilkan kalor. Reaksi yang terjadi adalah :
2 Al(s) + 2 KOH(aq) + 6 H2O(liq) ---> 2 KAl(OH)4(aq) + 3H2(g)
2Al(s) + 2OH-(aq) + 6H2O(liq) ---> 2Al(OH)4-(aq) + 3H2(g)
Dalam reaksi ini terbentuk gas H2 yang ditandai dengan munculnya gelembung- gelembung gas. Gelembung-gelembung gas hilang setelah semua aluminium bereaksi. Setelah didiamkan dan didinginkan, disaring endapan yang filtratnya ditampung dengan menggunakan erlenmeyer. Selanjutnya filtrat yang ada di erlenmeyer itu ditambahkan larutan asam sulfat sebanyak 30 ml. Reaksi yang terjadi adalah :
2 KAl(OH)4(aq) + H2SO4(aq) ---> 2 Al(OH)3(s) + K2SO4(aq) + 3 H2O-
Al(OH)4- (aq) + H+(aq) ---> Al(OH)3(s) + H2O(liq) Tujuan penambahan larutan H2SO4 dilakukan agar seluruh senyawa K[Al(OH)4] dapat bereaksi sempurna. Al(OH)3 yang terbentuk langsung bereaksi dengan H2SO4 dengan persamaan reaksi sebagai berikut :
2 Al(OH)3(s) + 3 H2SO4(aq) ---> Al2(SO4)3 (aq) + 6 H2O(liq)
Al(OH)3 (s) + 3H+ (aq) ---> Al3+(aq) + 3H2O (liq)Selanjutnya setelah terbentuk endapan lalu disaring kembali dan dicuci dengan menggunakan etanol bertujuan untuk menyerap kelebihan air dan mempercepat pengeringan.
Tawas yang berkualitas baik memiliki ciri-ciri berbentuk bongkahan dan tidak berwarna (bening). Dari percobaan yang kami lakukan, ternyata limbah kaleng dapat menghasilkan tawas yang berbentuk seperti kristal bening, tawas yang didapat itu merupakan tawas murni. Pada alumunium foil juga menghasilkan sejumlah tawas, tawas tersebut berbentuk serbuk halus berwarna putih.
Tawas yang telah dibuat ini kemudian diuji keberhasilannya dalam menjernihkan air. Air merupakan salah satu komponen yang sangat penting bagi kehidupan selain udara. Makhluk hidup yang ada tidak dapat lepas dari penggunaan air dalam kehidupannya. Namun pada akhir-akhir ini persoalan ketersediaan air bersih menjadi suatu masalah karena banyaknya air yang telah kerkotori oleh kontaminan. Kontaminan-kontaminan berasal dari limbah rumah tangga dan industri. Sehingga secara kualitas, sumberdaya air telah mengalami penurunan. Demikian pula secara kuantitas, yang sudah tidak mampu memenuhi kebutuhan yang terus meningkat. Koagulasi dan flokulasi merupakan suatu proses yang umum dilakukan dalam pengolahan limbah cair industri. Koagulasi adalah proses penambahan bahan kimia atau koagulan kedalam air limbah yang bertujuan untuk mengurangi daya tolak menolak antar partikel koloid, sehingga partikel-partikel tersebut dapat bergabung menjadi flok-flok kecil. Flokulasi adalah proses penggabungan flok-flok kecil sehingga menjadi flok-flok yang lebih besar sehingga akan mudah mengendap. Tawas ditambahkan ke dalam air sehingga menyebabkan partikel-partikel tersuspensi akan mengendap dan kemudian air dapat diolah lebih lanjut. Salah satunya dengan proses filtrasi. Kemudian didesinfeksi lalu dapat dikonsumsi.
Untuk menguji tawas yang telah dibuat dapat dilakukan dengan menggunakan air limbah (air yang sudah tidak jernih lagi) yaitu dengan cara tawas ditambahkan dengan koagulan, koagulan tersebut memiliki kemampuan untuk menjadikan partikel koloid tidak stabil sehingga partikel siap membentuk flok. Disini air yang digunakan untuk dijernihkan adalah air selokan sekitar PLT dan larutan FeCl3. Kurang lebih 2 ml masing-masing air selokan dan larutan FeCl3 itu dimasukkan dalam tabung reaksi. Kemudian diberi tawas dan dihomogenkan. Terlihat bahwa air selokan yang semula berwarna keruh itu kemudian menjadi agak bening setelah diberi tawas. Hasilnya terlihat pada gambar dibawah ini :
Berikut adalah hasil tawas yang kami peroleh :
VII Kesimpulan
VIII Daftar Pustaka